ثورة في علاج أمراض المناعة: حين أعادت هندسة الخلايا رسم حدود المستحيل
في التاسع من أبريل 2026، نشرت مجلة Med -ذراع الطب السريري لدى Cell Press، أعرق دور النشر العلمي في العالم-دراسةً وصفها المختصون بأنها من أكثر الحالات الطبية إثارةً في تاريخ علم المناعة التطبيقي الحديث. صاحبة الدراسة امرأة ألمانية في السابعة والأربعين من عمرها، عانت قرابة عقد كامل من ثلاثة أمراض مناعية ذاتية في آنٍ معاً، وجرّبت تسعة أنواع مختلفة من العلاجات دون جدوى، حتى باتت حياتها معلّقة بنقل دم يومي. ثم جاء علاج واحد فأنهى المعاناة كلها في سبعة وعشرين يوماً.
جدول المحتويات
هذه ليست قصة عجيبة معزولة. إنها نافذة مفتوحة على مستقبل الطب المناعي، وعلى إمكانية أن يُعاد تصميم جهاز المناعة البشري من داخله، كما يُعاد تصميم برنامج حاسوبي معطوب.
ثلاثة أمراض تنقلب على صاحبتها
لكي يفهم القارئ عمق هذا الإنجاز، لا بد أن يدرك طبيعة الكارثة التي كانت تعيشها هذه المريضة. كانت تعاني في وقت واحد من ثلاثة اضطرابات مناعية تبدو متناقضة في طبيعتها، لكنها تشترك في جذر واحد.
المرض الأول هو فقر الدم الانحلالي المناعي (Autoimmune Hemolytic Anemia — AIHA)، وهو حالة تهاجم فيها أجسام مضادة أنتجها جهاز المناعة نفسُه خلايا الدم الحمراء وتدمّرها. الدم الذي ينقل الأكسجين إلى كل خلية في الجسم يصبح هدفاً للجسم ذاته. كانت هذه المريضة تحتاج كل يوم إلى دم جديد من المتبرعين لتبقى حية، لأن جهازها المناعي لا يكفّ عن تدمير خلاياها الحمراء.
المرض الثاني هو نقص الصفائح المناعي (Immune Thrombocytopenia — ITP)، وفيه يستهدف الجهاز المناعي الصفائح الدموية المسؤولة عن وقف النزيف. والصفائح الدموية هي “قوات الإنقاذ” في الدم؛ حين تُجرح إصبعك، هي من تتسابق لسدّ الجرح. حين تختفي بفعل هجوم مناعي، يصبح أي نزيف بسيط تهديداً حقيقياً للحياة.
المرض الثالث هو متلازمة الأجسام المضادة للفوسفوليبيد (Antiphospholipid Antibody Syndrome — APLAS)، وهو على النقيض تماماً من المرض السابق: بدلاً من زيادة خطر النزيف، يرفع هذا الاضطراب خطر تكوّن الجلطات الخطيرة في الأوردة والشرايين. جهاز مناعي يقلل الصفائح من جهة، ويرفع خطر الجلطات من جهة أخرى، تناقض مأساوي داخل جسد واحد.
الجامع المشترك بين الأمراض الثلاثة، وهذه هي النقطة المحورية في الدراسة، هو أنها جميعاً أمراض تقودها الخلايا البائية (B cells). هذه الخلايا البيضاء التي يُنتجها نخاع العظام هي مصنع الأجسام المضادة في الجسم. حين تعمل بشكل سليم، فهي درعٌ واقٍ ضد البكتيريا والفيروسات. حين تصاب بخلل، تتحوّل إلى مصنع لأسلحة تستهدف الجسم نفسه.
عقدٌ من الأدوية.. وتسعة إخفاقات
منذ عام 2014، خاضت هذه المريضة معارك مضنية مع المرض. تسعة خطوط علاجية متتالية -تضمنت الكورتيزون، ومثبطات المناعة، والأجسام المضادة وحيدة النسيلة، وعلاجات أخرى- لم تُفلح في إيقاف زحف المرض. حين وصلت إلى عيادة البروفيسور فابيان مولر في مستشفى إرلانغن الجامعي عام 2025، كانت تحتاج إلى نقل دم يومي وعلاج مضاد للتخثر بصفة مستمرة لتجنّب الجلطات. كلمة “مقاوم للعلاج” Refractory التي يستخدمها الأطباء في وصف حالتها تُترجَم في الواقع إلى معنى أقسى: لم يتبقَّ ما يمكن تجربته.
غير أن البروفيسور مولر وفريقه كانوا يتابعون عن كثب تجربةً علاجية بدأت تشق طريقها من عالم أورام الدم نحو آفاق أوسع: علاج CAR-T.
من السرطان إلى المناعة: إعادة اختراع أداة جراحية
علاج CAR-T اختصار لـ Chimeric Antigen Receptor T-cells أو “الخلايا التائية ذات المستقبلات الخيمرية”، لم يكن في أصله مصمَّماً لأمراض المناعة الذاتية. طُوِّر ليكون سلاحاً في وجه السرطانات الدموية، وتحديداً تلك التي تنشأ من تحوّل الخلايا البائية إلى خلايا سرطانية كاللمفوما واللوكيميا. وقد حقق في هذا الميدان نتائج وُصفت بالثورية.
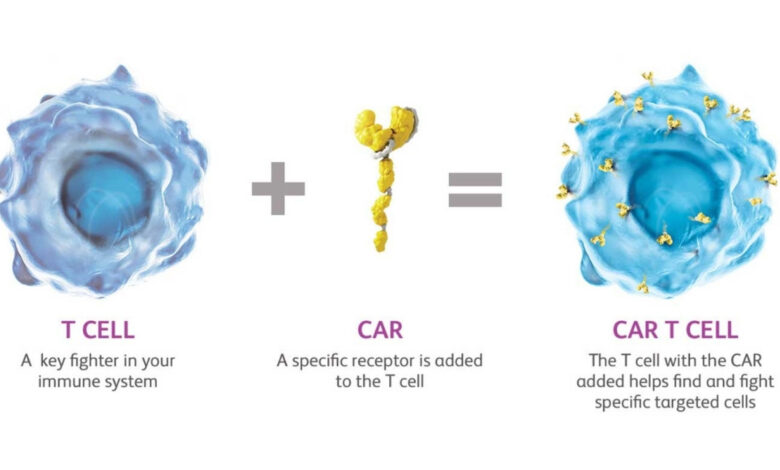
المبدأ الجوهري للعلاج قابل للفهم حتى دون خلفية علمية: يقوم الأطباء بسحب خلايا T من دم المريض نفسه، ثم يعيدون هندستها وراثياً في المختبر لتكتسب مستقبلاً جديداً على سطحها يجعلها قادرة على التعرف على هدف محدد ومهاجمته، ثم تُحقن من جديد في الجسم. في حالات سرطانات الدم، يكون الهدف هو الخلايا السرطانية. وفي حالة المناعة الذاتية المدفوعة بالخلايا البائية، يصبح الهدف هو الخلايا البائية المارقة.
البروتين الذي اختاره فريق إرلانغن كهدف للخلايا المُعدَّلة هو CD19، وهو بروتين يتربّع على سطح الخلايا البائية في مختلف مراحل نضجها. لأن هذه الخلايا التائية المُصمَّمة تستطيع الانتشار في مختلف أنسجة الجسم والوصول إلى الخلايا البائية المعطوبة سواء في مراحل النضج أو في مراحل النمو، فإنها تنجح في تطهير الجسم منها على نحو شامل.
الدواء المستخدم في هذه الحالة تحديداً هو Zorpocabtagene autoleucel المعروف اختصاراً بـ Zorpo-cel وهو أحد أحدث التركيبات من فئة CAR-T الموجَّهة ضد CD19. خضعت المريضة أولاً لبروتوكول تحضيري من العلاج الكيميائي يشمل فلوداربين وسيكلوفوسفاميد لاستنزاف الخلايا التائية الموجودة، ثم أُعطيت جرعة من الخلايا المُعدَّلة بمعدل مليون خلية لكل كيلوغرام من وزن الجسم. كل هذا في إطار “الاستخدام الرحيم” Compassionate Use، أي خارج بروتوكول تجربة سريرية رسمية، بموافقة لجنة أخلاقيات البحث وبإذن خطي من المريضة.
سبعة أيام كافية
ما جرى بعد ذلك جعل حتى الأطباء المشاركين يصفونه بـ”اللافت بشكل استثنائي”. في اليوم السابع فقط من تلقّي العلاج، توقفت المريضة عن الحاجة إلى نقل الدم. وفي غضون خمسة وعشرين يوماً، عادت مستويات الهيموغلوبين — وهو البروتين الحامل للأكسجين في الدم — إلى نطاقاتها الطبيعية مع اختفاء علامات انحلال الدم.
لكن الإنجاز لم يتوقف عند حدود المرض الأول. الأجسام المضادة للفوسفوليبيد التي كانت ترفع خطر الجلطات انخفضت تدريجياً حتى أصبحت سلبية تماماً، دون أي ارتداد طوال أحد عشر شهراً من المتابعة. وتحسّنت أعداد الصفائح الدموية وتثبّتت دون الحاجة إلى أي علاج إضافي.
الأهم من كل ذلك: حين عادت الخلايا البائية للظهور بعد أشهر في الجسم، كانت جميعها تقريباً من النوع “الساذج” naive cells، أي خلايا جديدة نظيفة لا تحمل ذاكرة مرضية ولا تنتج أجساماً مضادة تهاجم الجسم. هذا يعني أن العلاج لم يُدمر الخلايا البائية المعطوبة فحسب، بل أتاح فرصة إعادة ضبط المنظومة المناعية من الصفر.
وصف البروفيسور فابيان مولر المشهد بعبارات لا تصدر عادةً من الوسط الأكاديمي الصارم: قال إن التدخل المبكر بهذا العلاج قد يمكّن في المستقبل من وقف المرض قبل وقوع أضرار عضوية لا يمكن تعويضها، وإعادة المريض إلى حياته قبل فوات الأوان.
قبل هذا الإنجاز بعام: الذئبة ومسار الرصيد
ليست حالة هذه المريضة منبتّةً عن سياقها العلمي. في عام 2022، وصف باحثون من مستشفى إرلانغن الجامعي نفسه خمسة مرضى مصابين بالذئبة الحمامية الجهازية المعندة على العلاج، حقّقوا هدأةً تامة بعد خضوعهم لعلاج CAR-T، وعاشوا دون أي علاج لما يزيد على سبعة عشر شهراً. بعض هؤلاء الباحثين أنفسهم هم من أشرفوا على الحالة الجديدة.
هذا يعني أن فريق إرلانغن لا يخطو في المجهول، بل يوسّع بشكل منهجي دائرة تطبيق مفهوم أثبت نجاحه، ليشمل أمراضاً مناعية متعددة كانت تُعدّ في ما مضى خارج نطاق الشفاء.
قيود حقيقية يجب ألّا تُخفى
الأمانة العلمية تقتضي ألّا تُقرأ هذه النتائج كإعلان عن علاج جاهز للتوزيع الشامل. الدراسة المنشورة في Med صريحة في هذا الشأن: هذه حالة واحدة، وتجربة فردية، ولا تُشكّل وحدها الحجة الكافية لاستخلاص نتائج قاطعة. يشدّد العلماء على أن الأمر يتطلب مزيداً من التجارب السريرية المضبوطة قبل اعتماد هذا العلاج على نطاق واسع.
يضاف إلى ذلك أن علاج CAR-T عملية معقدة ومكلفة. تتضمن تصنيع خلايا معدَّلة لكل مريض على حدة، مما يجعل التوسع فيها أمراً غير يسير. وتبلغ تكلفة علاج CAR-T في حالات السرطان نحو نصف مليون دولار. كما أن المرضى يحتاجون إلى مرحلة تحضيرية بالعلاج الكيميائي لاستنزاف خلاياهم المناعية الموجودة، مما يضيف قدراً من الخطر إلى العملية. كل هذه العوامل تجعل هذا العلاج في طوره الراهن مناسباً للحالات الحرجة والمقاومة للعلاجات التقليدية، لا للحالات المتوسطة.
بيد أن هذه القيود ليست ذريعة لتقليل الأهمية المبدئية للاكتشاف، بل هي خارطة الطريق نحو ما هو قادم.
ما الذي يفتحه هذا الباب؟
يذهب الباحثون في مجال المناعة اليوم إلى أن ما حدث في إرلانغن يحمل دلالة أعمق من مجرد شفاء امرأة واحدة. إنه دليل على صحة مفهوم جوهري: أن كثيراً من أمراض المناعة الذاتية -التي طالما وُصفت بأنها “غير قابلة للشفاء” وأقصى ما يمكن عمله هو “السيطرة عليها”- هي في حقيقتها أمراض ناجمة عن خلل في مجموعة محددة من الخلايا، وأن محو هذا الخلل من جذره ثم منح الجهاز المناعي فرصة لإعادة بناء نفسه قد يُفضي إلى هدأة حقيقية لا إلى مجرد كبح مؤقت.
المدى الذي تصل إليه هذه الرؤية مبشّرٌ: أمراض كالذئبة الحمامية الجهازية، والتصلب المتعدد، والتهاب المفاصل الروماتويدي المعند، ومتلازمة شوغرن، وسواها من الأمراض المناعية التي تُقيّد ملايين البشر، كلها مدرجة اليوم على قائمة البحث التطبيقي لهذا المنهج العلاجي. التجارب السريرية تتوسع، ومؤشر الأمل يرتفع.
خاتمة
في العلم كما في التاريخ، ثمة لحظات لا تبدو في وقت وقوعها سوى خطوة فنية متواضعة، لكنها تُعيد رسم ما كان يُظنّ حدوداً ثابتة. ما جرى في مستشفى إرلانغن الجامعي في مطلع عام 2025، ونُشر على الملأ في أبريل 2026، هو واحدة من تلك اللحظات.
لم تشفَ تلك المرأة لأنها محظوظة. شفيت لأن عقوداً من البحث في علم المناعة وعلاجات السرطان التقت في لحظة واحدة مع سؤال بسيط: وإن حوّلنا هذا السلاح نحو الخلايا المارقة في الأمراض المناعية، ماذا سيحدث؟
الجواب جاء سريعاً وعميقاً. والعلم الآن يصغي.
المصادر العلمية:
- Korte, I.K. et al. “CD19 CAR-T therapy induces remission in refractory autoimmune hemolytic anemia with ITP and antiphospholipid syndrome.” Med, Cell Press, نُشر أونلاين 9 أبريل 2026. DOI: 10.1016/j.medj.2026.101075
- مستشفى إرلانغن الجامعي، جامعة فريدريش ألكسندر إرلانغن-نورنبرغ، ألمانيا
- EurekAlert / AAAS — البيان الصحفي الرسمي للدراسة، أبريل 2026





